外科手术设备一旦开始使用,便容不得丝毫妥协。
每寸设计、材料的每次选择、可用性的每个要素,均可能直接影响患者的治疗效果。在英国IDC,我们深知在术中那些关键时刻,医护人员所仰赖的正是手术器械的精准度、无菌性和易用性。
凭借超过50年的医疗器械设计与开发经验,我们的项目经验涵盖了广泛的外科领域,从微创手术器械到专业手术室系统。团队将创新设计思维与严谨的工程实践及深厚的法规专业知识相结合,确保外科手术设备在关键场合表现完美。

通过将开发流程集中于同一体系下,我们减少了各阶段间沟通不畅的风险,并确保每个设计决策都能提升产品的最终性能。无论是开发可重复使用的手术工具还是复杂的一次性器械,我们的重点都是提供能满足严苛临床需求的稳健解决方案。

我们遵循IEC 62366标准,并从一开始就将MDR和FDA的合规要求融入设计流程,从而在使用便捷性证据的获取和法规审批方面做到前置,而非事后追加。这确保了外科手术设备不仅精准,而且安全、符合人体工学、易于使用。
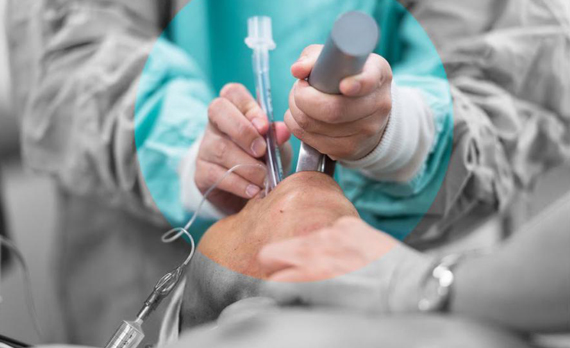
例如我们与瑞奇外科合作的超声刀手持式手柄设计,在投产前的大规模临床试用中,可用性受到了临床医生极高的评价,也成为该系列产品的关键卖点之一;

我们与BD合作的穿刺套件实现了该品类全球首个可调节角度的刚性鞘管,使得部件同时拥有了灵活性和坚韧;
我们开发的妇科消融系统采用仿生设计思路,解决了消融头开合形态的准确性及灵活性需求;
我们与美敦力合作的吻合器适本土化设计,让产品实现了针对中国临床端使用更好的人机工学特征、更吸引力的外观,及更合理的成本。

每件外科产品都存在固有风险,从潜在的操作失误到灭菌挑战。我们的流程遵循ISO 14971,在开发的每个阶段实施风险管理。我们及早识别危害,尽可能从工程上消除风险,并完整记录所有控制措施,以实现全面的法规可追溯性。
IDC的英国设计室设施包括用于无菌产品装配的洁净室,以及用于精密制造的可控环境。这意味着我们能够以与大规模生产相同的无菌性要求,对外科手术设备进行原型制作、测试和改进。
从选择生物相容性材料到确保与灭菌工艺的兼容性,我们从第一天起就着手解决制造要求。这种设计与生产能力的整合,确保了在整个开发过程中,设备性能、无菌性和成本效益都能得到平衡。