随着国内外医疗器械行业监管法规的日趋严谨,中国药监部门对企业违规行为查处力度加大、对产品的审查要求愈发趋于严谨和规范化。彼时,市场上医疗器械产品同质化愈发严重,全新的医疗器械产品包装、结构设计、人因考量等因素越来越多的被企业重视,医疗器械产品设计开发合规再造成为行业关注的焦点。
在近两年公布的国家局、各省局飞行检查结果中,设计开发多出现缺陷,越来越多的企业开始意识到,在医疗器械产品开发过程中合规的重要性。为帮助医疗器械企业提升设计开发合规意识做好医疗器械产品战略的制定,深圳市医疗器械产业联盟联合致众科技股份有限公司、英国IDC产品化机构、中城新产业控股有限公司、深圳市生命科学产业服务有限公司拟于2018年5月31日举办“医疗器械新产品战略制定与设计开发合规研讨会”。
主办单位:
深圳市医疗器械产业联盟
承办单位:
致众科技股份有限公司
中城新产业控股有限公司
深圳市生命科学产业服务有限公司
活动时间:2018年5月31日(周四)
活动地点:坪山区聚龙山A路与聚龙山B路交汇处 深城投&中城 生命科学园二楼报告厅
时间议程:
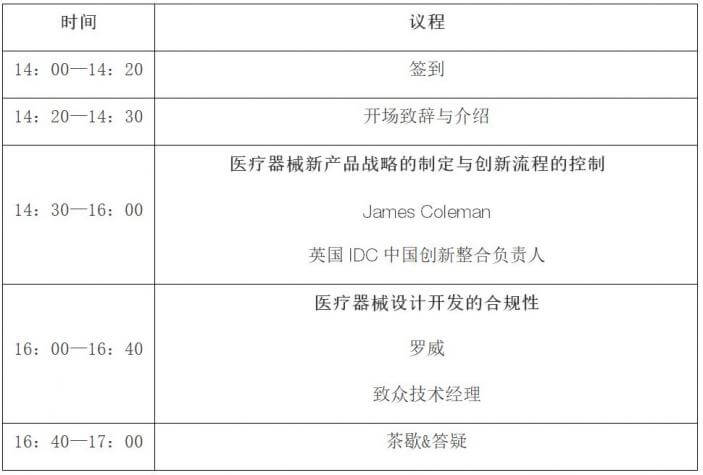
1、医疗器械产品战略组成元素
2、医疗器械产品前期研究与专利战略
3、医疗器械用户研究及人因工程
4、医疗器械设计开发的技术研究
5、CFDA对医疗器械产品设计开发的法规要求
6、医疗器械设计开发流程的设计意图把控
 英国IDC创新整合负责人 James Coleman
英国IDC创新整合负责人 James Coleman
拥有拉夫堡大学工业设计和技术学位,James作为高级设计工程师,具备超过 10余年的产品开发经验,包括从概念、工程到后期生产。他曾就职于著名的国际品牌Dyson的英国、中国及马来西亚分公司。在医疗领域,James专注于以严谨详尽的方式解决设计及技术问题,通过最佳的实践技术将产品从概念阶段成功的开发为产品。专注于消费电子及医疗设备的创新,James推动着IDC中国区的设计及工程整合工作。
参与研发的医疗产品举例: 可调节患者座椅系统,压力温度控制垫,行走器,安全采血笔,动态血糖监测仪等。
 致众技术经理 罗威
致众技术经理 罗威
罗经理拥有华中科技大学工学学士,管理学硕士-质量管理方向,曾在某国际医疗设备研发制造厂商从事八年质量管理工作,历任研发QA、设备QA、软件QA、体系QA、资深质量项目经理等职。主导过生命信息与支持、医学影像、体外诊断类医疗器械的风险分析、技术法规、质量管理、软件信息集成等流程体系的建立。中国注册体系考核、欧盟CE认证审核、美国FDA审厂、巴西、韩国等全球质量管理体系检查,项目策划与现场应对经验丰富。主持并参与了超声内镜、质子放疗、眼科设备等海归创新创业项目、研究单位成果转化的医疗器械注册、质量管理体系构建,在注册技术资料撰写咨询、体系规划、问题分析等方面见解独到,合规高效推进产品上市进程。
公益活动不收取任何费用,参会代表请携带名片。
活动联系人:包女士
bao.di@idc.cn.com
021-33315511-200
请注明“深圳设计开发研讨会”字样
报名截止时间:2018年5月30日中午12点
为切实解决企业在日常工作中的问题,本活动设有答疑环节,欢迎大家带着问题前来。